Această cercetare, condusă de Dr. Qiu Ju, Qin Jun și Qiu Jinxin de la Institutul de Nutriție și Sănătate din Shanghai al Academiei Chineze de Științe, a fost publicată în Jurnalul de Alergie și Imunologie Clinică pe 17 septembrie.
Astmul este o boală respiratorie cronică la nivel mondial, determinată de supraactivarea imunității de tip 2. Un tip de celule imune innăscute numite „ILC2” joacă un rol central în acest proces, răspunzând rapid la stimuli ambientali și inducând direct inflamația căilor respiratorii. După expunerea inițială la alergeni, ILC2 pot intra într-o stare de „memorie”. Odată cu re-expunerea la doze mici de alergen sau semnale inflamatorii (cum ar fi IL-33), acestea se activează rapid și se proliferă extensiv, declanșând o inflamație „secundară” mai intensă. Acesta este un motiv crucial pentru care astmul este recurent și greu de tratat. Cu toate acestea, mecanismele epigenetice subiacente care guvernează această capacitate de memorie rămân neclare.
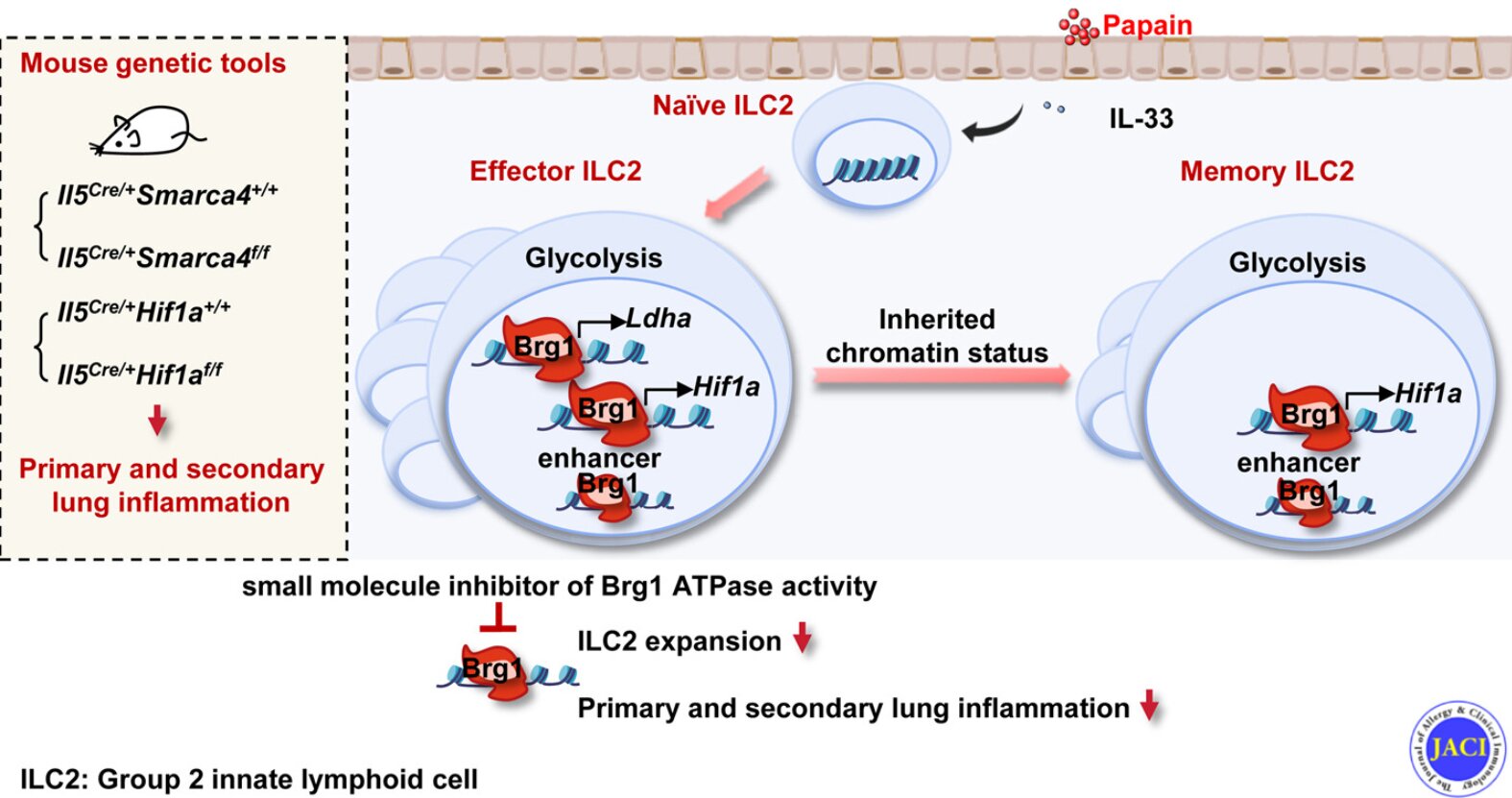
Prin analize multi-omic, cercetătorii au descoperit că expresia Brg1 (codificată de Smarca4), un component de bază al complexului de remodelare a cromatinei mSWI/SNF, a fost semnificativ supraexprimată într-un model de șoarece cu inflamație pulmonară alergică. Citokina inflamatorie IL-33, un semnal cheie care induce activarea ILC2 în astm, a indus direct expresia Brg1 în ILC2, sugerând că Brg1 ar putea fi un „comutator cheie” pentru activarea ILC2.
Experimentele ulterioare au demonstrat că în timpul activării ILC2, Brg1 se leagă și deschide o serie de regiuni cromatice, în special loci genetice legate de metabolismul celular. De remarcat, Brg1 promovează procesul glicolitic în ILC2 prin îmbunătățirea accesibilității cromatinei a genelor metabolice cheie precum Hif1a și Ldha, susținând astfel expansiunea și supraviețuirea acestora.
Cercetătorii au descoperit, de asemenea, că această „amprentă metabolică” modelată de Brg1 poate fi reținută de la ILC2 efectori la ILC2 de memorie, permițând celulelor de memorie să mențină nivele ridicate de activitate glicolitică și capacitate rapidă de răspuns în momentul re-expunerii la alergeni. În modelele animale, eliminarea specifică a Smarca4 sau Hif1a în ILC2 a inhibat semnificativ proliferarea ILC2 și a ameliorat atât inflamația pulmonară acută, cât și cea secundară, demonstrând că Hif1α este o moleculă cheie care leagă Brg1 de

Editor RevistaSanatatii.ro. Isi doreste ca activitatea lui sa aduca speranta milioanelor de oameni bolnavi din Romania, sa le aline suferintele si sa le ofere speranta.